
Abstrak
Matriks ekstraseluler asli menunjukkan struktur alur dan tonjolan multiskala yang terus berubah, seperti nanogroove berbasis fibril kolagen dalam jaringan tulang, dan mengatur respons seluler. Namun, peralihan dinamis antara nanostruktur alur dan tonjolan pada tingkat molekuler belum ditunjukkan. Di sini, bahan yang mampu melakukan peralihan alur-tonjolan dinamis pada skala puluhan nanometer dikembangkan dengan menggabungkan secara fleksibel nanoridge (MAN) yang dapat diaktifkan secara magnetis oleh RGD ke nanogroove nonmagnetik dengan lebar yang disetel secara independen yang sebanding dengan ukuran filopodia penyaji integrin dengan memodulasi hidrofobisitas dalam mikroemulsi bikontinu, yang memungkinkan modulasi siklik aksesibilitas RGD dan adhesi seluler. Nanogroove dengan lebar sedang membatasi aksesibilitas RGD dalam keadaan “alur” tempat RGD-MAN terkubur, yang dibalik dengan mengangkatnya secara magnetis untuk menonjol dan membentuk keadaan “tonjolan” yang sepenuhnya mengekspos RGD. Hal ini secara reversibel menstimulasi perekrutan integrin, perakitan kompleks adhesi fokal, mekanotransduksi, dan diferensiasi sel punca secara in vivo. Ini adalah demonstrasi pertama dari nanostruktur alur dan punggungan tingkat molekuler yang menunjukkan kemampuan peralihan yang belum pernah terjadi sebelumnya antara nanostruktur alur dan punggungan. Penyetelan serbaguna dari lebar, tinggi, kemiringan, dan bentuk struktur nanogroove yang rumit dengan manipulasi jarak jauh dapat mencerahkan pemahaman tentang interaksi sel-ligan skala molekuler untuk perawatan penuaan, cedera, dan penyakit terkait stres berbasis rekayasa sel punca.
1 Pendahuluan
Dalam jaringan asli, matriks ekstraseluler (ECM) memiliki struktur alur dan punggungan yang kompleks dan dinamis di berbagai skala yang berinteraksi secara rumit dengan sel untuk mengatur fungsi jaringan, homeostasis, dan regenerasi. [ 1 – 3 ] Struktur ini secara langsung atau tidak langsung mengatur sel dengan mengubah sifat fisik atau komposisi ECM. [ 4 , 5 ] Pada skala makro, korteks serebral otak menunjukkan daerah lipatan sulkus (alur) dan girus (punggungan), [ 6 ] di mana lebar alur sulkus meningkat secara dinamis seiring bertambahnya usia. [ 7 ] Peningkatan dinamis dalam lebar alur tersebut berkorelasi terbalik dengan fungsi kognitif pada gangguan neurologis seperti skizofrenia [ 8 ] dan penyakit Alzheimer. [ 9 , 10 ] Sulkus dan girus mengekspresikan komponen ECM secara berbeda, termasuk protein perekat sel (misalnya, kolagen dan fibronektin), [ 11 ] yang memengaruhi pelipatan korteks dan respons neuronal. [ 12 ] Khususnya, neuron yang dipisahkan oleh punggung girus menunjukkan konektivitas fungsional yang lebih besar daripada neuron yang dipisahkan oleh alur sulkus. [ 13 ] Pada skala mikro, membran dasar pada kulit menunjukkan struktur alur dan punggung yang dinamis [ 14 , 15 ] yang terus-menerus direnovasi sebagai respons terhadap penuaan dan stresor eksternal (misalnya, paparan sinar ultraviolet), yang meningkatkan aktivitas metaloproteinase matriks, sehingga mengakibatkan degradasi kolagen. [ 16 ] Perubahan dinamis ini membentuk kembali ceruk sel punca dengan mengubah komposisi dan mekanika ECM untuk mengatur proliferasi dan diferensiasi sel punca, sehingga memodulasi respons sel punca. [ 17 – 19 ]
Sebagai struktur alur dan punggungan skala nano, ECM permukaan tulang memiliki alur nano berbasis fibril kolagen [ 20 ] yang terus-menerus direnovasi untuk mempertahankan homeostasis tulang. [ 21 – 23 ] Selama proses renovasi ini, sel punca berinteraksi secara dinamis dengan motif ligan Arg-Gly-Asp (RGD) yang bersifat adhesif sel di ECM berbasis kolagen [ 24 , 25 ] yang mengatur adhesi dan diferensiasi sel, yang menentukan sifat mekanis dan integritas fungsional jaringan tulang. [ 26 , 27 ] Biasanya, sel berinteraksi dengan ECM berbasis kolagen melalui filopodia dinamis, yang merupakan tonjolan membran plasma penyaji integrin ramping dengan diameter di atas 60 nm. [ 28 ] Struktur ini memfasilitasi pengenalan dan pengikatan reseptor integrin (≈10 nm) ke RGD yang ada pada fibril kolagen. [ 29 ] Pada sel punca, pengikatan dinamis tersebut menginduksi pengelompokan integrin dan pematangan adhesi fokal, yang sangat penting untuk mekanotransduksi. [ 30 – 32 ] Interaksi ini memulai jalur pensinyalan yang mengatur adhesi sel punca, diferensiasi, dan regenerasi jaringan. [ 33 , 34 ] Oleh karena itu, merancang biomaterial yang meniru nanostruktur alur dan punggungan dinamis sangat penting untuk memajukan pemahaman tentang interaksi sel punca-material dan regulasinya secara in vivo.
Penelitian ekstensif telah dilakukan untuk meniru struktur alur dan punggungan ECM asli di berbagai skala (yaitu, skala makro, [ 35 – 38 ] skala mikro, [ 39 – 43 ] dan skala nano) [ 44 – 47 ] untuk menyelidiki efek pengaturan selnya. Berbagai struktur alur dan punggungan statis spesifik skala pada skala makro, [ 36 ] skala mikro, [ 39 ] dan skala nano [ 45 ] telah dikembangkan untuk pola organoid, pengaturan sel yang bergantung pada kelengkungan, dan migrasi sel yang terkait dengan lebar saluran, masing-masing. Namun, tidak satu pun dari pendekatan ini yang memungkinkan modulasi struktur pada skala puluhan nanometer, apalagi kontrol dinamisnya (Tabel S1 , Informasi Pendukung). Meskipun ada kemajuan ini, pengembangan struktur alur dan punggungan pada skala puluhan nanometer, yang sesuai dengan skala molekul integrin dalam filopodia yang penting untuk regulasi sel tingkat molekuler, masih belum dieksplorasi. [ 48 ] Lebih jauh, kendali jarak jauh ligan dapat lebih meniru sifat dinamis nanostruktur ECM. [ 49 – 52 ] Kelompok kami baru-baru ini menunjukkan penggunaan medan magnet untuk memanipulasi nanomaterial bulat [ 46 ] atau memanjang [ 53 ] yang memodulasi derajat pemblokiran ligan dalam struktur alur dan punggungan “skala nano” dan untuk mengendalikan nano komposit hierarkis yang menunjukkan anisotropi ligan skala ganda “nano-” dan “mikro-“. [ 54 ] Namun, tidak ada penelitian sebelumnya yang mencapai regulasi peralihan dinamis antara nanostruktur alur dan punggungan. Cahaya baru-baru ini digunakan untuk memediasi puntiran struktur alur-punggungan “skala makro” [ 38 ] atau peralihan antara struktur alur dan punggungan “skala mikro”, [ 43 ] tetapi keduanya tidak memungkinkan regulasi peralihan dinamis antara nanostruktur alur dan punggungan. Temuan terkini ini menunjukkan perlunya pengembangan material baru yang menunjukkan kemampuan peralihan alur versus punggungan yang dinamis pada skala puluhan nanometer yang mewakili dinamika skala molekuler.
Di sini kami menyajikan bahan yang dapat dialihkan secara dinamis dengan struktur alur puluhan nanometer yang menggunakan templat nanogroove non-magnetik dengan berbagai lebar nanogroove (50, 80, dan 110 nm, yang masing-masing bersesuaian dengan lebar nanogroove Kecil, Sedang, dan Besar) yang mana nanoridges yang dapat diaktivasi secara magnetis (MAN) yang menyajikan RGD dikonjugasikan pada kepadatan yang sama di seluruh kelompok melalui penghubung fleksibel yang panjang (Gambar S1 , Informasi Pendukung). Lebar nanogroove disetel secara independen, sambil mempertahankan ukuran dan bentuk templat nanogroove, melalui modulasi berbasis alkohol amfifilik dari hidrofobisitas dalam tetesan mikroemulsi bikontinu. Lebar nanogroove, sebanding dengan diameter filopodia sel penyaji integrin (>60 nm), menunjukkan perbedaan lebar antar yang mirip dengan molekul integrin dan skala perpindahannya (≈30 nm). [ 55 , 56 ] Nanogroove kecil (50 nm) menghalangi adhesi seluler dalam keadaan “groove”, mungkin karena kesulitan filopodia dalam mengakses RGD akibat kendala spasial, yang hanya dapat diatasi sebagian hingga tingkat yang tidak signifikan dalam keadaan “ridge” dengan mengaktifkan (menaikkan) RGD-MAN secara magnetis ( Gambar 1a ). Lebih jauh lagi, nanogroove besar (110 nm) memungkinkan adhesi seluler yang kuat dalam keadaan “groove” karena filopodia dapat dengan mudah mengakses RGD, yang tetap dapat diakses dalam keadaan “ridge” yang sedikit terpengaruh oleh peningkatan RGD-MAN secara magnetis. Sebaliknya, nanogroove sedang (80 nm) kurang mendukung adhesi seluler dalam keadaan “groove”, karena filopodia memiliki akses terbatas ke RGD yang terkubur yang dapat menonjol dari pola nanogroove untuk membentuk “ridge” dari RGD yang terekspos sepenuhnya dengan meningkatkan RGD-MAN secara magnetis. Aktivasi tersebut menghasilkan perekrutan integrin aktif, pengelompokan integrin, perakitan kompleks adhesi fokal, dan diferensiasi yang dihasilkan (Gambar 1a ).
Gambar 1
Buka di penampil gambar
Kekuatan Gambar
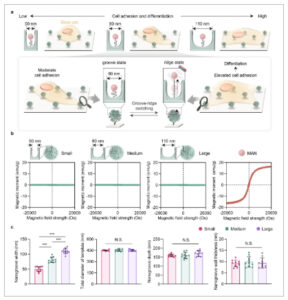
Demonstrasi skematis dan eksperimental dari penelitian ini. a) Dalam RGD-MAN-nanogrooves, kelompok nanogroove yang lebih besar lebih unggul daripada lebar nanogroove yang lebih kecil dalam hal aksesibilitas sel punca ke RGD, yang mengarah pada peningkatan adhesi dan diferensiasi sel punca. Dalam keadaan “alur” tanpa aplikasi magnetik, RGD-MAN-nanogrooves dengan lebar nanogroove sedang menunjukkan adhesi sel punca sedang. Sebaliknya, dalam keadaan “punggungan”, di mana RGD-MAN dimanipulasi ke atas secara reversibel untuk menonjol dan membentuk punggungan dengan menempatkan magnet permanen di sisi atas bahan, adhesi sel punca dan diferensiasi berikut dipromosikan. b) Karakteristik magnetik templat nanogroove dengan lebar nanogroove yang berbeda dan MAN diverifikasi dengan vibrating sample magnetometry (VSM). c) Kuantifikasi lebar nanogroove, diameter templat total, kedalaman nanogroove, dan ketebalan dinding antar-nanogroove. Data ditampilkan sebagai mean ± standard error ( n = 10). Tanda bintang yang ditunjukkan pada rentang nilai p (***: p < 0,001) menunjukkan perbedaan yang signifikan secara statistik. NS menunjukkan perbedaan yang tidak signifikan secara statistik.
Kami menyajikan material pertama yang menunjukkan struktur alur dan punggungan pada skala filopodia dan molekuler integrin (yaitu, skala puluhan nanometer). Ini juga merupakan laporan pertama yang menunjukkan peralihan dinamis antara nanostruktur alur dan punggungan untuk regulasi sel yang efektif in vivo. Studi saat ini berbeda dari studi sebelumnya yang melaporkan regulasi sel oleh struktur alur dan punggungan statis pada skala makro, [36 ] skala mikro , [ 39 ] dan skala nano, [ 45 ] dan dari studi terbaru yang menunjukkan modulasi dinamis struktur alur dan punggungan skala makro [ 38 ] dan skala nano [ 46 ] tanpa mengatur “peralihan” dinamis antara struktur alur dan punggungan, serta peralihan dinamis antara struktur alur dan punggungan skala mikro [ 43 ] , tetapi tidak pada “skala nano.” Kemampuan untuk memodulasi konfigurasi alur dan punggungan secara siklis pada skala molekuler melalui medan magnet menyediakan alat yang menjanjikan untuk mempelajari interaksi dinamis antara sel dan nanostruktur alur dan punggungan yang kompleks. Terobosan ini menggarisbawahi pentingnya pengendalian dinamika ligan tingkat molekuler dan memajukan pemahaman kita tentang regulasi seluler dinamis in vivo menuju aplikasi pengobatan berbasis sel punca untuk cedera traumatis dan penyakit terkait penuaan dan stres.
2 Hasil dan Pembahasan
2.1 Penyetelan Independen Lebar Nanogroove Mengatur Rekrutmen Integrin
Untuk menganalisis efek perbedaan skala molekuler dalam lebar nanogroove pada regulasi sel punca, templat nanogroove dengan lebar alur yang bervariasi pada skala puluhan nanometer (sebanding dengan skala filopodia penyaji integrin, ≈60 nm) [ 28 ] disiapkan. Templat ini dikembangkan dengan cermat untuk menampilkan lebar alur yang bervariasi sebesar 50 nm (“Kecil”), 80 nm (“Sedang”), dan 110 nm (“Besar”) sambil mempertahankan ukuran dan bentuk templat yang konstan. Perbedaan antar lebar spesifik ini selaras dengan perpindahan integrin skala molekuler (≈30 nm) [ 55 , 56 ] untuk memodulasi interaksi antara kendala spasial skala nano dan adhesi seluler yang dimediasi integrin.
Untuk tujuan ini, pola nanogroove disintesis menggunakan tetesan mikroemulsi bikontinu yang mengandung saluran minyak dan air yang distabilkan oleh surfaktan dan alkohol amfifilik. Saluran minyak berfungsi sebagai pola spasial untuk kondensasi silika (Si), dengan lebarnya dikontrol dengan memanfaatkan secara strategis panjang rantai hidrofobik dari alkohol amfifilik yang digunakan: heksanol (alur 50 nm), heptanol (alur 80 nm), atau oktanol (alur 110 nm). Meningkatnya sifat hidrofobisitas alkohol amfifilik memperluas saluran minyak, sehingga menghasilkan alur yang lebih besar. Biasanya, penyetelan lebar alur yang independen seperti itu pada ukuran pola yang konstan terbatas karena perbedaan panjang rantai alkohol amfifilik juga memengaruhi ukuran pola keseluruhan. [ 57 , 58 ] Sementara tetraetil ortosilikat (TEOS), prekursor Si, dihidrolisis pada antarmuka minyak–air dan terkondensasi dalam saluran air, sehingga membentuk dinding nanogroove berbasis silika, batasan sebelumnya diatasi dengan mengoptimalkan secara tepat hidrofobisitas alkohol amfifilik yang memodulasi lebar saluran minyak sebagai ruang kosong antara alur di bawah hidrofobisitas yang berbeda (Gambar S2a , Informasi Pendukung).
Analisis morfologi dan unsur dari templat nanogroove melalui mikroskop elektron transmisi (TEM), spektroskopi dispersif energi (EDS), dan mikroskop elektron pemindaian (SEM) mengungkapkan lebar alur yang berbeda sebesar 50,4 ± 8,5 nm (“Kecil”), 81,1 ± 9,1 nm (“Sedang”), dan 109,9 ± 8,9 nm (“Besar”). Semua templat secara eksklusif terdiri dari elemen Si yang tidak aktif secara magnetis (Gambar 1b,c dan Gambar S2b,c , Informasi Pendukung). Total diameter templat (450 nm), kedalaman alur (165 nm), dan ketebalan dinding antar-nanogroove (9,5 nm) tetap konstan di semua kelompok, yang mengonfirmasi bahwa lebar alur adalah satu-satunya variabel yang disetel secara independen (Gambar 1c ).
Bahasa Indonesia: Untuk memungkinkan peralihan dinamis antara alur nanoskala dan struktur punggungan, nanoridges yang dapat diaktifkan secara magnetis (MAN) dikembangkan dan dikonjugasikan ke templat nanogroove (MAN-nanogrooves) menggunakan polimer fleksibel panjang [poli(etilen glikol); penghubung PEG] diikuti oleh penggandengan RGD (RGD-MAN-nanogrooves) (Gambar S3a,b , Informasi Pendukung). MAN direkayasa untuk memungkinkan konjugasi bahkan dalam templat nanogroove “Kecil” (lebar alur 50 nm) dengan melapisi nanopartikel Fe3O4 7 nm ( inti MAN) dengan cangkang SiO2 untuk mencapai ukuran akhir 30 nm, setelah itu mereka di-PEGilasi dan dikonjugasikan ke templat nanogroove pada kepadatan yang sama di semua kelompok di bawah reaksi jenuh (Gambar S4a,b , Informasi Pendukung). Karakterisasi melalui TEM, hamburan cahaya dinamis (DLS), TEM resolusi tinggi (HR-TEM), TEM pemindaian resolusi tinggi (HR-STEM), dan analisis difraksi area terpilih (SAED) dari inti MAN dan MAN secara kolektif mengungkapkan morfologi bulat homogen dengan karakteristik kristal Fe3O4 yang dipertahankan setelah pelapisan cangkang SiO2 (Gambar S4a –c dan S5 , Informasi Pendukung). Magnetometri sampel bergetar (VSM) menunjukkan bahwa templat nanogroove tidak aktif secara magnetis, sedangkan inti MAN dan MAN menunjukkan reversibilitas magnetik tinggi yang cocok untuk aktivasi magnetiknya (Gambar 1b dan Gambar S6 , Informasi Pendukung).
Selanjutnya, MAN-nanogrooves dengan lebar alur yang bervariasi digabungkan secara independen ke permukaan material pada kerapatan pola yang konstan, dengan MAN dilapisi secara serial dengan RGD perekat sel (Gambar S7 , Informasi Pendukung). Untuk tujuan ini, MAN fungsionalisasi amina pertama-tama di-PEGilasi melalui ikatan amida, kemudian dikonjugasikan ke pola nanogroove ber-thiolated (pola MAN-nanogroove), yang digabungkan ke permukaan material sebelum dilapisi dengan RGD (Gambar S8a,b , Informasi Pendukung). Kelompok fungsional maleimide terminal pada permukaan material yang tidak bereaksi dengan pola RGD-MAN-nanogroove dengan cepat dihidrolisis menjadi asam maleamat yang tidak reaktif, mencegah adhesi sel yang tidak spesifik. [ 59 ] Perubahan dalam ikatan kimia karakteristik dan muatan permukaan setelah setiap langkah modifikasi mengonfirmasi keberhasilan fungsionalisasi serial melalui spektroskopi inframerah transformasi Fourier dan pengukuran potensi zeta (Gambar S8a,b,S9a,b , dan S10a–c , Informasi Pendukung). Analisis morfologi dan unsur templat MAN-nanogroove melalui analisis TEM dan EDS memvalidasi keberhasilan konjugasi MAN dalam templat nanogroove, dengan distribusi MAN yang seragam di seluruh kelompok dengan lebar alur yang bervariasi (Gambar S11a,b dan S12 , Informasi Pendukung).
Setelah memverifikasi sintesis yang berhasil, perbedaan skala molekuler dalam nanogroove dengan lebar yang bervariasi diuji untuk mengetahui efeknya pada perekrutan integrin sel dan pengikatan untuk regulasi sel punca pada permukaan material ( Gambar 2a–c ). Sel punca mesenkimal manusia (hMSC; Lonza, nomor katalog: PT-2501) dipilih sebagai model karena kesamaan ukuran antara templat nanogroove (≈450 nm) dan kompleks adhesi fokal (≈500 nm), yang penting dalam mengatur mekanotransduksi dan diferensiasi sel punca. [ 30 , 60 , 61 ] Dalam penelitian ini, sel hanya disemai satu kali pada awal kultur di semua kelompok. Setelah 48 jam, pewarnaan imunofluoresens dilakukan untuk memvisualisasikan protein yang terlibat dalam adhesi sel dan mekanotransduksi (Gambar 2b,c dan Gambar S13 , Informasi Pendukung). Khususnya, jumlah RGD-MAN per templat dan kerapatan templat pada bahan serta kerapatan RGD konstan di semua kelompok, memastikan keseragaman (Gambar 2d dan Gambar S14 , Informasi Pendukung). Selain itu, tidak ada MAN yang terletak di atas dinding nanogroove, kemungkinan karena lebar dinding tidak mencukupi (≈9,5 nm) untuk menopang MAN berukuran 30 nm secara stabil (Gambar 2d ).
Gambar 2
Buka di penampil gambar
Kekuatan Gambar
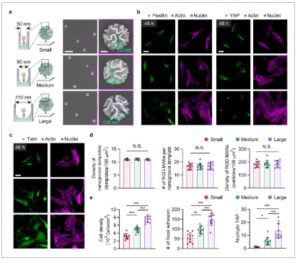
Rekayasa lebar alur nano RGD-MAN-nanogrooves mengatur sel punca. a) Gambar SEM dari bahan yang menyajikan alur nano MAN dengan lebar alur nano yang berbeda [batang skala: 1 µm (perbesaran rendah) dan 100 nm (perbesaran tinggi)]. Gambar confocal dari sel punca yang melekat yang diimunostain secara fluoresensi untuk b) paxillin atau YAP, c) atau talin dengan nukleus dan F-actin setelah 48 jam kultur pada alur nano RGD-MAN dengan lebar alur nano yang berbeda (batang skala: 50 µm). d) Kuantifikasi kepadatan templat alur nano, jumlah RGD-MAN per templat alur nano, dan kepadatan RGD-MAN. e) Kuantifikasi kepadatan sel yang melekat, jumlah adhesi fokal, dan rasio YAP nukleus/sitoplasma. Data ditampilkan sebagai mean ± standard error [(c,d) n = 10]. Tanda bintang yang ditetapkan pada rentang nilai p (*: p < 0,05; **: p < 0,01; ***: p < 0,001) menunjukkan perbedaan yang signifikan secara statistik. NS menunjukkan perbedaan yang tidak signifikan secara statistik.
Gambar imunofluoresensi sel punca yang melekat pada pola nanogroove dengan lebar alur yang bervariasi menunjukkan bahwa adhesi sel meningkat secara proporsional dengan peningkatan lebar alur. Kelompok “Kecil” menunjukkan ekspresi minimal integrin β1, paxillin, talin, dan F-actin dan kepadatan sel yang melekat rendah, jumlah adhesi fokal, dan luas sel, yang semuanya meningkat secara signifikan dalam kelompok “Besar”, bersama dengan penurunan faktor bentuk (sumbu sel mayor/minor) (Gambar 2e dan Gambar S15 , Informasi Pendukung). Tren serupa diamati untuk mekanotransduser yang dimediasi adhesi YAP, yang rasio nuklir terhadap sitoplasma meningkat dengan peningkatan lebar nanogroove. Pengaturan perekrutan integrin seperti itu dalam cetakan nanogroove dengan lebar alur yang bervariasi selanjutnya dikonfirmasi oleh gambar SEM sel induk yang mengalami pelabelan integrin β1 dengan nanopartikel Au 15 nm (AuNP), yang menunjukkan jumlah AuNP pelabelan integrin β1 yang jauh lebih tinggi yang mengindikasikan peningkatan perekrutan integrin dengan meningkatnya lebar nanogroove (Gambar S16a,b dan S17a–c , Informasi Pendukung).
Temuan-temuan ini secara kolektif menunjukkan bahwa perekrutan integrin β1, yang memediasi adhesi sel, terutama dipengaruhi oleh lebar alur nano skala molekuler yang sebanding dengan filopodia yang menyajikan integrin. [ 28 ] Peningkatan adhesi sel punca dan mekanotransduksi pada alur yang lebih besar (“Sedang” dan “Besar”) kemungkinan besar merupakan hasil dari kemampuan mereka untuk mengakomodasi infiltrasi filopodia, sementara kelompok “Kecil” tidak memiliki ruang yang cukup untuk pengikatan integrin. Dengan demikian, rekayasa alur nano skala molekuler menyediakan strategi yang layak untuk mengatur adhesi yang dimediasi integrin dan mekanotransduksi dalam sel punca.
Untuk memvalidasi efek pengaturan spesifik RGD, eksperimen kontrol dilakukan tanpa MAN dalam templat nanogroove atau MAN-nanogroove tanpa pelapisan RGD (Gambar S18a,b dan S19a,b , Informasi Pendukung). Perlunya RGD untuk pengaturan sel punca ditunjukkan oleh adhesi sel yang tidak didukung pada material polos dan di seluruh kelompok MAN-nanogroove tanpa pelapisan RGD. Tidak seperti penelitian sebelumnya yang melaporkan efek perbedaan kelengkungan permukaan pada respons seluler, [ 62 , 63 ] tingkat adhesi sel yang serupa di seluruh kelompok tanpa pelapisan RGD menunjukkan bahwa perbedaan kelengkungan permukaan akibat lebar alur yang bervariasi memiliki efek yang tidak signifikan. Temuan ini menggarisbawahi peran penting pelapisan RGD dalam pengaturan sel punca yang tepat dalam nanostruktur alur.
2.2 Pengalihan Dinamis antara Alur dan Punggungan Nanoskala untuk Pengaturan Sel Punca
Selanjutnya kami menyelidiki efek pengalihan dinamis RGD-MAN dari status “groove (G)”, di mana mereka terkubur dalam pola nanogroove, ke status “ridge (R)”, di mana RGD-MAN diaktifkan secara magnetis (diangkat) untuk menonjol dari nanogroove, yang memaparkan RGD untuk menstimulasi respons sel punca (Gambar S20 , Informasi Pendukung). Untuk mengaktifkan RGD-MAN secara magnetis dengan menaikkannya ke status “ridge”, magnet permanen (305 mT) ditempatkan di atas permukaan material. Gambar imunofluoresensi sel punca yang dikultur pada kelompok “Medium” dalam status “ridge” selama 48 jam mengungkapkan peningkatan organisasi F-actin dan paxillin secara nyata, dengan peningkatan yang signifikan dalam kepadatan sel, jumlah adhesi fokal, dan luas sel serta penurunan faktor bentuk dibandingkan dengan yang dikultur dalam status “groove” (Gambar S21a,b , Informasi Pendukung).
Sebaliknya, kelompok “Kecil” menunjukkan tingkat adhesi sel punca yang rendah baik dalam keadaan “alur” maupun “punggung bukit”, tanpa perbedaan yang signifikan secara statistik. Demikian pula, kelompok “Besar” menunjukkan tingkat adhesi sel punca yang tinggi secara konsisten di kedua keadaan, tanpa perbedaan yang nyata di antara keduanya (Gambar S21a,b , Informasi Pendukung). Temuan ini menunjukkan bahwa lebar alur 50 nm dari kelompok “Kecil” tidak cukup untuk memfasilitasi perekrutan dan pengikatan integrin yang efektif ke RGD-MAN, bahkan setelah aktivasi magnetik ke keadaan “punggung bukit”. Sebaliknya, lebar alur 110 nm dari kelompok “Besar” cukup lebar untuk mendukung pengikatan integrin jenuh dan adhesi sel dalam keadaan “alur”, sehingga paparan RGD tambahan dalam keadaan “punggung bukit” menjadi kurang efektif. Oleh karena itu, peralihan dinamis antara struktur alur dan punggungan skala nano melalui aktivasi magnetik RGD-MAN memiliki efek regulasi paling menonjol dalam kelompok “Sedang” dengan lebar alur 80 nm, yang sedikit melebihi ukuran filopodia penyaji integrin (≈60 nm). Dengan demikian, kelompok “Sedang” dipilih untuk pemeriksaan lebih lanjut tentang efek peralihan alur nano-ke-punggungan siklik pada regulasi sel punca dalam penelitian ini.
Untuk memvalidasi efek pengaturan spesifik peralihan alur-punggung RGD skala nano dinamis, serangkaian eksperimen kontrol dilakukan. Pertama, untuk menilai apakah peralihan dinamis alur dan alur nanostruktur bergantung pada aktivasi magnetik, nanopunggung yang tidak dapat diaktifkan secara magnetik (MIN) berukuran 30 nm yang seluruhnya terdiri dari SiO2 disintesis dan dikonjugasikan ke templat nanogroove (MIN-nanogroove) (Gambar S22a–c dan S23a,b , Informasi Pendukung). Dengan tidak adanya inti MAN, RGD-MIN di seluruh kelompok lebar nanogroove tidak menunjukkan efek pengaturan apa pun pada sel punca, dengan tingkat adhesi tetap konstan antara status “alur” dan “punggung” di setiap kelompok, terlepas dari upaya aktivasi magnetik ke status “punggung” (Gambar S24a,b , Informasi Pendukung). Konjugasi langsung RGD-MAN ke templat nanogroove tanpa penghubung fleksibel juga tidak memengaruhi tingkat adhesi sel punca (Gambar S25a,b , Informasi Pendukung). Hasil-hasil ini menegaskan bahwa respons magnetik MAN dan fleksibilitas penghubung sangat penting untuk memungkinkan peralihan yang tepat antara keadaan “alur” dan “punggung” RGD-MAN, sehingga memungkinkan pengaturan adhesi sel punca yang dinamis dan cermat.
2.3 Pengalihan Siklus Alur dan Punggungan Nanoskala untuk Pengaturan Diferensiasi Sel Punca
Selanjutnya kami merenungkan apakah peralihan dinamis antara nanostruktur alur dan punggungan melalui aktivasi magnetik RGD-MAN dapat dikontrol secara siklis untuk mengatur diferensiasi sel punca. Pertama, pencitraan mikroskopi gaya atom yang dilakukan in situ dan profil tinggi linier yang sesuai memverifikasi bahwa MAN yang awalnya dalam keadaan “alur (G)” dapat dinaikkan ke keadaan “punggungan (R)” setelah aktivasi magnetik secara siklis: 418,4 nm (keadaan “G” pertama), 438,9 nm (keadaan “R” pertama), 418,2 nm (keadaan “G” kedua), 437,0 nm (keadaan “R” kedua), dan 419,3 nm (keadaan “G” ketiga) (Gambar S26 , Informasi Pendukung). Perbedaan tinggi rata-rata antara MAN dalam keadaan “alur” dan dalam keadaan “punggungan” adalah 19,3 nm, sedangkan tinggi templat nanogroove non-magnetik tetap tidak berubah sepanjang kontrol siklik.
Untuk menyelidiki apakah peralihan alur-punggung siklik ini mengarah pada regulasi siklik adhesi sel punca, sel punca dikultur pada kelompok “Sedang” sementara aktivasi magnetik dihentikan atau dilanjutkan setiap 24 jam hingga 72 jam, yang menghasilkan empat kondisi: “GGG,” “GRG,” “RGR,” dan “RRR”. Gambar imunofluoresensi menunjukkan regulasi siklik adhesi sel punca dengan ekspresi integrin yang meningkat, kepadatan sel yang melekat, jumlah adhesi fokal, dan ukuran sel dalam sel yang dikultur dalam kondisi yang berakhir pada keadaan “R”, yang semuanya berkurang dalam sel yang dikultur dalam kondisi yang berakhir pada keadaan “G”, disertai dengan peningkatan faktor bentuk (Gambar S27a,b dan S28a,b , Informasi Pendukung). Pengaturan siklik ini selanjutnya divalidasi oleh gambar SEM sel induk yang diberi label dengan AuNP pelabelan integrin β1, yang menunjukkan jumlah AuNP pelabelan integrin β1 yang jauh lebih tinggi, yang menunjukkan peningkatan rekrutmen integrin, dalam keadaan “ridge” dibandingkan dalam keadaan “groove” (Gambar S29a–c , Informasi Pendukung).
Karena perekrutan integrin dan pematangan adhesi fokal mendorong transduksi mekano sel punca dan diferensiasi osteogenik, selanjutnya kami meneliti efek peralihan alur-ke-punggung siklik pada proses ini dengan membudidayakan hMSC pada kelompok “Medium” dalam medium penginduksi diferensiasi osteogenik ( Gambar 3a ). Konsisten dengan regulasi yang diamati untuk adhesi sel, gambar imunofluoresensi mengungkap translokasi nuklir YAP dan RUNX2 yang secara signifikan lebih tinggi pada kelompok yang berakhir pada status “R” peralihan alur-punggung siklik daripada pada kelompok yang berakhir pada status “G” (Gambar 3a–c ). Analisis western blot pada sel punca setelah peralihan alur-punggung siklik semakin menguatkan hasil ini, dengan ekspresi RUNX2 yang nyata (penanda osteogenik awal) dan osteokalsin (penanda osteogenik akhir) pada sel punca yang dikultur dalam kondisi yang berakhir pada status “R” (Gambar 3d–f ).
Gambar 3
Buka di penampil gambar
Kekuatan Gambar
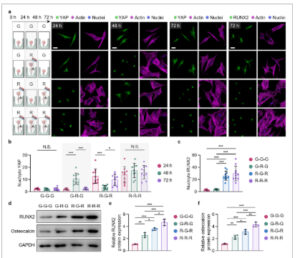
Konversi siklik dari alur/punggung skala nano RGD mengendalikan diferensiasi sel punca. a) Gambar konfokal sel punca yang melekat yang diimunostain secara fluoresensi untuk YAP atau RUNX2 dengan nuklei dan F-aktin setelah 24, 48, atau 72 jam pembudidayaan pada alur nano RGD-MAN dengan lebar alur nano sedang sambil mengubah atau mempertahankan status dinamis alur nano RGD-MAN setiap 24 jam pembudidayaan (batang skala: 50 µm). b) Kuantifikasi rasio YAP nuklir/sitoplasma setelah 24, 48, atau 72 jam selama peralihan siklik antara alur skala nano RGD dan status pungung. c) Kuantifikasi rasio RUNX2 nuklir/sitoplasma setelah 72 jam peralihan siklik antara alur skala nano RGD dan status pungung. d) Gambar Western blot dan kuantifikasi protein e) RUNX2 dan f) osteocalcin dalam sel induk yang melekat setelah 72 jam peralihan siklik antara alur dan keadaan punggungan skala nano RGD. Data ditampilkan sebagai rata-rata ± standar error ( n = 10). Tanda bintang yang ditetapkan pada rentang nilai p (*: p < 0,05; **: p < 0,01; ***: p < 0,001) menunjukkan perbedaan yang signifikan secara statistik. NS menunjukkan perbedaan yang tidak signifikan secara statistik.
Untuk memverifikasi bahwa regulasi siklik diferensiasi dimediasi oleh mekanotransduksi terkait adhesi, sel punca dikulturkan dengan adanya salah satu inhibitor berikut yang menargetkan jalur adhesi utama: ML-9 (inhibitor kinase rantai ringan miosin), Swinholide A (inhibitor polimerisasi aktin), atau Y27632 [inhibitor kinase protein terkait rho (ROCK)] (Gambar S30a–d,S31a,b , dan S32a,b , Informasi Pendukung). Kelompok yang diobati dengan inhibitor menunjukkan rasio nukleus/sitoplasma YAP dan RUNX2 yang berkurang secara signifikan, bahkan pada kelompok yang diakhiri dengan status “R”, yang menunjukkan bahwa efek peralihan alur-ke-punggung siklik pada adhesi dan mekanotransduksi secara efektif dinetralkan. Hasil-hasil ini menyoroti peran kinase rantai ringan miosin, polimerisasi aktin, dan pensinyalan ROCK dalam mekanotransduksi dan diferensiasi yang dimediasi adhesi sel punca, yang dapat dialihkan secara siklis melalui transisi alur-ke-punggung skala nano yang reversibel (Gambar S30a–d, S31a, b , dan S32a, b , Informasi Pendukung).
2.4 Pengalihan Reversibel Alur dan Punggungan Nanoskala untuk Mengatur Diferensiasi Sel Punca In Vivo
Untuk menyelidiki potensi pengendalian jarak jauh peralihan alur-punggung skala nano untuk mengatur diferensiasi sel punca secara in vivo, sel punca disuntikkan ke bahan yang ditanamkan secara subkutan yang menyajikan RGD-MAN-nanogroove pada tikus (Gambar S33 , Informasi Pendukung). Untuk memastikan adhesi sel yang stabil tanpa kebocoran atau kerusakan material, tikus dipertahankan dalam anestesi selama peralihan alur-punggung dinamis. Untuk pengendalian peralihan, magnet permanen (305 mT) ditempelkan ke bagian belakang setiap tikus dengan selotip bedah. Magnet dilepaskan atau dipertahankan setelah 3 jam hingga 6 jam, menghasilkan kondisi berikut: “GG,” “GR,” “RG,” dan “RR.” Gambar imunofluoresensi sel punca yang melekat menunjukkan tingkat adhesi sel punca dan translokasi nuklir YAP dan RUNX2 yang meningkat secara signifikan, yang menunjukkan peningkatan mekanotransduksi dan diferensiasi osteogenik, masing-masing, dalam kelompok di mana RGD-MAN dialihkan secara magnetis ke keadaan “ridge” dibandingkan dengan kelompok yang berakhir dalam keadaan “groove” ( Gambar 4a dan S34a,b dan S35a,b , Informasi Pendukung). Ko-lokalisasi inti sel dengan antigen nuklir spesifik manusia (HuNu) selanjutnya mengonfirmasi adhesi dan diferensiasi yang dimediasi mekanotransduksi dari sel punca manusia yang disuntikkan pada bahan yang ditanamkan (Gambar 4a ).
Gambar 4
Buka di penampil gambar
Kekuatan Gambar
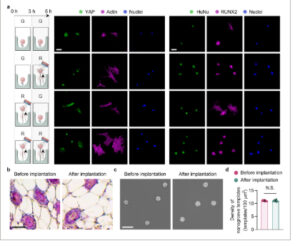
Pengalihan reversibel dari status alur/punggung skala nano RGD memodulasi diferensiasi sel punca secara in vivo. a) Gambar konfokal sel punca yang melekat yang diimunostain secara fluoresensi untuk YAP dengan nuklei dan F-aktin, atau RUNX2 dengan nuklei dan antigen nuklei spesifik manusia (HuNu) pada 6 jam setelah implantasi (batang skala: 50 µm). Mode dinamis alur nano RGD-MAN diubah atau dipertahankan pada 3 jam setelah implantasi. b) Gambar mikroskop optik jaringan subkutan yang diwarnai hematoksilin dan eosin (H&E) di sekitar lokasi implantasi sebelum dan 6 jam setelah implantasi (batang skala: 200 µm). c) Gambar SEM bahan yang menyajikan alur nano RGD-MAN sebelum implantasi dan 6 jam setelah implantasi (batang skala: 1 µm), beserta d) kuantifikasi kepadatan templat alur nano. Data ditampilkan sebagai rata-rata ± kesalahan standar ( n = 10). NS menunjukkan perbedaan yang tidak signifikan secara statistik.
Analisis histologis jaringan yang dikumpulkan di sekitar lokasi implantasi dan dari organ yang jauh (jantung, limpa, ginjal, dan hati) menunjukkan toksisitas lokal dan sistemik yang tidak signifikan, memvalidasi keamanan dan biokompatibilitas bahan yang diimplan (Gambar 4b dan Gambar S36 , Informasi Pendukung). Gambar SEM dengan pengukuran kepadatan templat MAN dan nanogroove berikut dari bahan yang diimplan 1 minggu setelah implantasi mengonfirmasi bahwa integritas struktural templat RGD-MAN-nanogroove dipertahankan, dengan konfigurasi alur-punggung yang stabil, selama periode percobaan (Gambar 2a,c dan 4c,d dan Gambar S14 dan S37 , Informasi Pendukung). Pembuatan nanostruktur alur dan punggungan 3D dengan kemampuan peralihan yang dinamis selanjutnya akan menjamin efektivitas jangka panjang bahan-bahan ini terhadap regenerasi jaringan berbasis sel punca. Temuan-temuan ini menggarisbawahi kemampuan peralihan alur-punggung nanoskala dinamis untuk mengatur adhesi dan diferensiasi sel punca secara in vivo, dengan demikian menyoroti potensinya sebagai strategi inovatif untuk terapi regenerasi jaringan untuk penuaan, cedera, dan penyakit.
3 Kesimpulan
Singkatnya, kami mengembangkan sistem material yang dapat dialihkan secara dinamis dari alur ke punggungan dalam skala nano yang mampu melakukan transisi reversibel antara status “alur” (dengan RGD yang terkubur) dan “punggungan” (yang memperlihatkan RGD) pada skala molekuler (yaitu, skala puluhan nanometer) menggunakan templat alur nano dengan lebar alur yang bervariasi (50, 80, dan 110 nm), yang mana alur nano yang dapat diaktifkan secara magnetis (MAN), yang menyajikan RGD pada kepadatan yang identik di seluruh kelompok, digabungkan melalui penghubung fleksibel yang panjang. Khususnya, keterbatasan sebelumnya dalam penyetelan lebar alur secara independen pada ukuran templat yang konstan diatasi untuk pertama kalinya dengan memanfaatkan sifat hidrofobisitas alkohol amfifilik yang optimal yang memodulasi lebar saluran minyak sebagai ruang kosong di antara alur. Dalam kondisi “alur”, nanogroove “Kecil” (lebar alur 50 nm) membatasi aksesibilitas RGD, menghambat perekrutan filopodia penyaji integrin, adhesi fokal, dan mekanotransduksi sel punca, sementara nanogroove “Besar” (lebar alur 110 nm) mendukung aksesibilitas RGD yang kuat, memungkinkan adhesi dan diferensiasi sel. Alur “Sedang” (80 nm) memberikan kondisi antara yang optimal dengan aksesibilitas RGD terbatas dalam kondisi “alur” yang ditingkatkan secara signifikan setelah aktivasi magnetik ke kondisi “punggungan” dengan secara fisik membentuk punggungan RGD-MAN yang terangkat.
Aktivasi magnetik reversibel secara siklis mengubah RGD-MAN dari keadaan “alur” ke keadaan “punggungan”, sehingga meningkatkan perekrutan integrin, pembentukan adhesi fokal, dan mekanotransduksi sel punca, termasuk translokasi nuklir YAP dan RUNX2 yang difasilitasi, dan diferensiasi osteogenik berikutnya. Studi in vivo mengonfirmasi regulasi sel punca yang kuat, dengan toksisitas lokal atau sistemik minimal, sementara integritas struktural material sebagian besar tetap utuh selama periode percobaan. Studi ini merupakan demonstrasi pertama dari peralihan alur-punggungan skala nano yang reversibel, yang memajukan pemahaman kita tentang interaksi sel-material yang dinamis pada tingkat molekuler. Kemampuan untuk menyetel dinamika skala nano secara tepat dengan memodulasi diameter dan bentuk templat serta lebar, tinggi, kedalaman, kemiringan, dan ketebalan dinding alur nano menawarkan jalan yang menjanjikan untuk mengembangkan terapi regeneratif guna mengatasi penuaan, cedera, dan penyakit terkait stres.
4 Bagian Eksperimen
Penyetelan Independen Lebar Nanogroove Menggunakan Amfifil dengan Hidrofobisitas Berbeda
Untuk mensintesis pola nanogroove dengan lebar yang disetel secara independen (pada skala puluhan nanometer) antara dinding nanogroove yang berdekatan, alkohol amfifilik dengan hidrofobisitas yang berbeda dipilih untuk mengatur secara tepat tingkat infiltrasi air ke dalam emulsi air/minyak/surfaktan bikontinu. Tetesan mikroemulsi bikontinu yang terdiri dari air, minyak, surfaktan, dan alkohol amfifilik mencakup saluran minyak dan air. Di dalam tetesan mikroemulsi bikontinu ini, prekursor yang terlarut dalam saluran minyak berdifusi ke antarmuka minyak-air dan dihidrolisis. Prekursor yang terhidrolisis kemudian bergerak ke saluran air, tempat mereka mengembun untuk membentuk silika. Akibatnya, saluran air dalam tetesan mikroemulsi bikontinu diisi dengan silika, yang merupakan dinding nanogroove, sementara meninggalkan saluran minyak sebagai ruang kosong di antara dinding nanogroove yang berdekatan. Dalam proses ini, peningkatan panjang rantai alkohol amfifilik meningkatkan sifat hidrofobisitas surfaktan, sehingga meningkatkan lebar saluran minyak (yaitu, lebar nanogroove) dalam tetesan mikroemulsi bikontinu.
Dengan demikian, pola nanogroove dengan lebar nanogroove yang disetel secara tepat yaitu 50 nm (Kecil), 80 nm (Sedang), dan 110 nm (Besar) disintesis. Pertama, 1 g cetyltrimethylammonium bromide (surfaktan) dan 2,7 g urea sebagai katalis basa dalam 15 mL air deionisasi (DI) diaduk pada 900 rpm untuk membentuk larutan homogen berair. Ke dalam larutan ini, campuran 25,6 mL sikloheksana (minyak) dan 15 mL alkohol amfifilik dengan panjang rantai yang bervariasi (yaitu, hidrofobisitas; heksanol untuk lebar nanogroove Kecil, heptanol untuk lebar nanogroove Sedang, dan oktanol untuk lebar nanogroove Besar) ditambahkan tetes demi tetes dengan pengadukan terus-menerus untuk membentuk tetesan mikroemulsi bikontinu yang berfungsi sebagai pola untuk pertumbuhan silika. Setelah 10 menit, 2,1 mL tetraetil ortosilikat (TEOS; prekursor Si) ditambahkan tetes demi tetes ke dalam tetesan mikroemulsi bikontinu, yang kemudian diaduk pada 900 rpm selama 30 menit untuk memungkinkan TEOS larut ke dalam saluran minyak dari tetesan mikroemulsi bikontinu. Setelah menaikkan suhu hingga 80 °C, tetesan diaduk selama 30 jam untuk menginduksi hidrolisis dan kondensasi TEOS dalam templat, menghasilkan templat nanogroove SiO2 . Suspensi templat nanogroove dicuci tiga kali dengan aseton dan dua kali dengan etanol menggunakan sentrifugasi. Untuk menghilangkan residu organik dari permukaan templat nanogroove, 4 mL HCl ditambahkan ke suspensi templat nanogroove, yang kemudian diaduk pada 900 rpm pada 80 °C selama 20 jam. Terakhir, templat nanogroove dicuci tiga kali dengan etanol dan didispersikan dalam 20 mL etanol.
Penyetelan Independen RGD-MAN-Nanogrooves untuk Berbagai Kelompok Lebar Nanogroove
Untuk mencapai peralihan reversibel antara alur nano-RGD dan keadaan punggungan, MAN dikonjugasikan secara fleksibel ke alur nano dari templat alur nano menggunakan penghubung fleksibel panjang poli(etilen glikol) (PEG, 10 kDa) untuk membentuk alur nano-MAN. Untuk tujuan ini, 3 mL MAN yang didispersikan dalam air DI dicampur dengan 3 mL air DI, 12 µL N,N-Diisopropiletilamina (DIPEA), dan 6 mg maleimida-PEG-N-hidroksi-suksinimida (Mal-PEG-NHS, M w: 10 kDa dari Polysciences). Setelah diaduk selama 16 jam dan dicuci tiga kali dengan air DI, MAN yang mengandung PEG diperoleh dan didispersikan dalam 24 mL air DI.
Untuk menggabungkan MAN yang terPEGilasi ke permukaan templat nanogroove, permukaan templat nanogroove difungsionalisasikan secara tiol. Pertama, 500 µL templat nanogroove SiO2 yang didispersikan dalam etanol dan 500 µL etanol tambahan dicampur, setelah itu 100 µL (3-merkaptopropil)trimetoksisilana (MPTMS) dan 10 µL 500 m m tris(2-karboksietil)fosfin hidroklorida (TCEP) ditambahkan. Campuran diaduk dalam gelap selama waktu reaksi 16 jam untuk kecil (50 nm), 12 jam untuk sedang (80 nm), dan 8 jam untuk templat nanogroove besar (110 nm) untuk memperoleh kepadatan MAN yang terpeGilasi yang serupa yang dikonjugasikan ke nanogroove dengan lebar yang bervariasi. Kemudian, suspensi dicuci dengan etanol dan air DI masing-masing tiga kali. Terakhir, 4 mL dari setiap suspensi cetakan nanogroove bertiol dicampur dengan 2 mL suspensi MAN berPEGylated dan 4 µL DIPEA dan diaduk selama 16 jam untuk menggabungkan MAN berPEGylated ke permukaan nanogroove melalui reaksi tiol-ena.
Analisis Statistik
Untuk memastikan konsistensi data, semua percobaan diulang lebih dari satu kali (nomor replikasi ditunjukkan dalam keterangan gambar sebagai “n = x ”). Rincian pra-pemrosesan data percobaan yang relevan disediakan dalam Informasi Pendukung. Data disajikan sebagai rata-rata ± simpangan baku. Perangkat lunak GraphPad Prism (versi 8.0.2) digunakan untuk analisis statistik. Perbandingan statistik berbagai kelompok dan penentuan signifikansi dilakukan dengan menggunakan analisis varians satu arah (ANOVA) dan uji post hoc Tukey-Kramer. Signifikansi statistik ditunjukkan oleh jumlah tanda bintang yang ditetapkan pada rentang nilai p (*: p < 0,05; **: p < 0,01; ***: p < 0,001).

